Polysaccharide – Cellulose, Stärke, Glykogen

in nur 12 Minuten? Du willst ganz einfach ein neues
Thema lernen in nur 12 Minuten?
-
 5 Minuten verstehen
5 Minuten verstehen
Unsere Videos erklären Ihrem Kind Themen anschaulich und verständlich.
92%der Schüler*innen hilft sofatutor beim selbstständigen Lernen. -
 5 Minuten üben
5 Minuten üben
Mit Übungen und Lernspielen festigt Ihr Kind das neue Wissen spielerisch.
93%der Schüler*innen haben ihre Noten in mindestens einem Fach verbessert. -
 2 Minuten Fragen stellen
2 Minuten Fragen stellen
Hat Ihr Kind Fragen, kann es diese im Chat oder in der Fragenbox stellen.
94%der Schüler*innen hilft sofatutor beim Verstehen von Unterrichtsinhalten.
Grundlagen zum Thema Polysaccharide – Cellulose, Stärke, Glykogen
In diesem Video geht es um Polysaccharide - ganz speziell um Cellulose, Stärke und Glykogen. Diese drei Vertreter der Polysaccharide werden vorgestellt und bezüglich ihrer Struktur und ihren Eigenschaften besprochen.
Transkript Polysaccharide – Cellulose, Stärke, Glykogen
Guten Tag und herzlich willkommen. In diesem Video geht es um Polysaccharide - Cellulose, Stärke, Glykogen. Als Vorkenntnisse solltet ihr solides Wissen über Monosaccharide und Disaccharide mitbringen. Die glykosidische Bindung ist euch ein Begriff. Ihr wisst, was eine 1-4 Verknüpfung ist. Euch ist bekannt, was eine α-glykosidische Bindung und eine β-glykosidische Bindung sind. Ihr habt euch eingehend mit D-Glucose, der D-Glucopyranose, den HAWORTH-Formeln und der Sesselschreibweise für Monosaccharide beschäftigt. Das Ziel des Videos ist es, euch Struktur und Eigenschaften von Cellulose, Stärke und Glykogen näher zu bringen. Ich habe das Video in 6 Abschnitte unterteilt.
- Systematik
- Baustein Glucose
- Cellulose
- Stärke
- Glykogen und
Zusammenfassung
Systematik Ein Polysaccharid-Molekül ist aus vielen einzelnen Monosaccharid-Molekülen aufgebaut. Die Zahl der Bausteine beläuft sich zwischen den Größenordnungen von 102 bis 105. Polysaccharide werden auch als Glykane bezeichnet. Sie zählen zu den Biopolymeren, genau wie Polypeptide und Nukleinsäuren. Eine Gruppe der Glykane wird durch die Homoglykane gebildet. Diese sind nur aus gleichen Bausteinen aufgebaut. Zu den Homoglykanen zählen die Cellulose, die Stärke und das Glykogen. Diese drei Glykane werden wir im Video besprechen. Heteroglykane hingegen sind aus verschiedenen Bausteinen zusammengesetzt. Heteroglykane sind Heparin, Hyaloronsäuren und Murein.
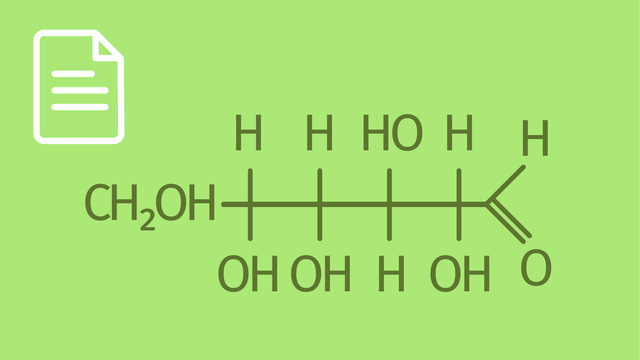
- Baustein Glucose Alle 3 Polysaccharide Cellulose, Stärke und Glykogen sind aus Glucose aufgebaut. Ich werde nun links das Glucosemolekül oben in HAWORTH-Schreibweise und darunter in Sesselform.Schreibweise aufzeichnen. Die Konfiguration ist richtig. Die Moleküle zeigen jeweils mit der Vorderseite zu uns. Die Hydroxygruppe am anomeren Kohlenstoffatom, rot gekennzeichnet, zeigt nach unten. In der Sesselformschreibweise kann man auch sagen, dass sie axial angeordnet ist. Bei diesem Molekül handelt es sich um α-D-Glucopyranose. Nun werde ich das entsprechende Anomer unter Benutzung der HAWORTH-Formel oben und der Sesselform-Schreibweise unten aufzeichnen. Die Moleküle zeigen mit der dick markierten Seite zu uns. Die Hydroxy-Gruppen sind bis auf eine Ausnahme genauso angeordnet, wie in der α-D-Glucopyranose. Der Unterschied besteht in der Stellung der Hydroxy-Gruppe am anomeren Kohlenstoffatom. In der HAWORTH-Formel ist sie nach oben gerichtet. In der Sesselform-Schreibweise ist sie nach rechts gerichtet. Sie hat eine äquatoriale Stellung bezüglich des Rings. Es handelt sich demnach um β-D-Glucopyranose. Sowohl Cellulose als auch Stärke und auch Glykogen sind alle aus Glucose aufgebaut. Cellulose besteht aus β-D-Glucopyranose. Stärke und Glykogen sind jeweils aus α-D-Glucopyranose aufgebaut.
- Cellulose Bei Cellulose handelt es sich um eine weißes geruchloses Pulver. Cellulose hat eine Dichte von etwa 1,5 g/cm³. Im Wasser ist sie unlöslich. Cellulose hat herausragende Bedeutung als Strukturmaterial der Pflanzen. Etwa 1012 t/Jahr werden auf- und abgebaut. Baumwolle besteht fast vollständig aus Cellulose. Etwa 1012 t/Jahr werden auf- und abgebaut. Das Molekül der Cellulose stellt eine unverzweigte Kette dar. Der Baustein der Cellulose ist die Cellobiose, die aus β-D-Glucopyranose aufgebaut ist. Die Verknüpfung zwischen den β-D-Glucopyranosemolekülen ist β-glykosidisch. Die Anzahl der Monosaccharidteilchen in der Kette ist in der Größenordnung von Tausend. Die biochemische Spaltbarkeit der Cellulose ist nur möglich in Anwesenheit des Enzyms Cellulase. Da der Mensch über keine Cellulase verfügt, ist die Cellulose für ihn nahrungstechnisch nicht verwendbar. Wiederkäuer hingegen besitzen Cellulase und können daher Cellulose verstoffwechseln. Dabei helfen ihnen symbiontische Bakterien im Verdauungstrakt.
- Stärke Stärke ist ein weißes, geruchloses Pulver. Etwa 1012 t/Jahr werden auf- und abgebaut. In der Literatur findet man allerdings auch Werte, die darunter liegen. Die Löslichkeit in Wasser ist schlecht. 50 g/l lösen sich bei einer Temperatur von 90 °C. Stärke ist für den Menschen eine Energiequelle. Wir finden sie in der Kartoffell zu etwa 82 % Stärke enthalten. Im Mais ist sie zu 71 % enthalten. Im Reis haben wir den höchsten Anteil an Stärke mit 89 %. Im Roggen sind 82 % Stärke enthalten. Stärke besteht aus den beiden Bestandteilen von Amylose und Amylopektin. Bei Amylose handelt es sich um ein unverzweigtes Polysaccharid. Amylopektin ist verzweigt. Eine gewisse Löslichkeit in Wasser ist bei Amylose vor allem beim Erwärmen vorhanden. Amylopektin ist wasserunlöslich. Die Anzahl der Bausteine beträgt bei Amylose in der Größenordnung von 102 bis 103. Bei Amylopektin sind mehr Bausteine enthalten. 103 bis weniger als 104. Die Glucosemoleküle sind in der Amylose als auch im Amylopektin durch α-glykosidische Bindungen miteinander verknüpft. Die biochemische Spaltbarkeit ist sowohl bei Amylose als auch beim Amylopektin gegeben. Stärke ist für den menschlichen Organismus nahrungsmitteltechnisch aufschließbar. Dafür sorgen entsprechende Enzyme, die sogenannten Amylasen. Die Besonderheit der Amylose besteht darin, dass sie eine Helix ausbildet. Darin können sich Jod-Moleküle einlagern. Es kommt zur Blaufärbung und man kann diese Reaktion für den Stärke- oder auch den Jodnachweis verwenden. Amylopektin besitzt durch seine Verzweigungen eine sogenannte Tannenbaumstruktur.
- Glykogen Glykogen hat eine dem Amylopektin ähnliche Struktur. Es ist nur stärker verzweigt. Bei Glykogen handelt es sich um das Reservepolysaccharid der Säugetiere und des Menschen. Die Glucosemoleküle sind untereinander durch α-glykosidische Bindungen verknüpft. Die Anzahl der Monosaccharid-Bausteine liegt in der Größenordnung von 105 bis weniger als 106. Biochemische Abbaubarkeit im menschlichen Organismus ist gewährleistet.
- Zusammenfassung Polysaccharide werden auch als Glykane bezeichnet. Man unterscheidet zwischen Homoglykanen und Heteroglykanen. Heteroglykane bestehen aus verschiedenen Bausteinen. Zu ihnen zählen Heparin, Hyaloronsäuren und Murein. Homoglykane bestehen nur aus gleichgearteten Bausteinen. In diesem Video haben wir Homoglykane, die nur aus D-Glucosemolekülen bestehen, betrachtet. Sowohl die α-, als auch die β-D-Glucopyranose kommen dabei zum Einsatz. Wir haben Cellulose, Stärke und Glykogen vorgestellt. Cellulose besitzt β-glykosidische Bindungen. Stärke und Glykogen hingegen α-glykosidische Bindungen. Aus diesem Grunde ist Cellulose für den menschlichen Organismus ernährungstechnisch nicht aufschließbar. Anders verhält es sich bei Stärke und Glykogen. Die Zahl der Bausteine beträgt bei Cellulose etwa 103 bis weniger als 104. Bei Amylose sind es in der Größenordnung von 102 bis 103. Amylopektin besteht aus 103 bis weniger als 104 Bausteinen. Bei Glykogen sind es noch mehr: 105 bis weniger als 106. Ich danke für die Aufmerksamkeit. Alles Gute. Auf Wiedersehen.
Polysaccharide – Cellulose, Stärke, Glykogen Übung
-
Beschreibe die Unterschiede zwischen Stärke und Glykogen.
TippsJe verzweigter das Polysaccharid, desto mehr Monomere sind enthalten.
LösungPolysaccharide aus D-Glucopyranosen haben sich bei fast allen Lebensformen als einer der Hauptspeicher für Energie entwickelt. Der Grund dafür ist, dass in diesem Polysacchariden direkt Glucosemoleküle gespeichert sind, die der Energielieferant für den Stoffwechsel sind. Bei tierischen Organismen haben sich Polysaccharide durchgesetzt, bei denen die Verknüpfung der Monmere über $\alpha$-glykosidische Bindungen erfolgt. Sie können auch nur diese verstoffwechseln.
Prinzipiell sind sich daher die Energiespeicher-Moleküle Amylose, Amylopektin und Glykogen sehr ähnlich, sie werden auch von den gleichen Enzymen verarbeitet. Die einzigen Unterschiede sind der Grad der Verzweigung und die Größe der Moleküle. Größe und Verzweigung nimmen von Amylose über Amylopektin bis hin zum Glykogen zu.
-
Benenne die Polysaccharide.
TippsBeachte den Typ der glykosidischen Bindung.
In welchem Molekül sind die Verzweigungen häufiger?
LösungDie vier Homoglykane, die aus D-Glucopyranose aufgebaut sind, unterscheiden sich in der Art der glykosidischen Bindung und im Grad der Verzweigung. Die einzige Verbindung mit einer $\beta$-glykosidischen Bindung ist die Cellulose. Dieses unverzweigte Molekül ist oben links dargestellt. Im Vergleich zu den anderen Molekülen ist deutlich erkennbar, dass es sich um eine $\beta$-glykosidische Bindung handelt, da diese in äquatorialer Stellung liegt.
Bei den anderen beiden Molekülen handelt es sich um verzweigte Moleküle mit $\alpha$-glykosidischen Bindungen. Im rechten Molekül sind die Verzweigungen häufiger, daher handelt es sich um Glykogen. Folglich ist das Molekül links unten Amylopektin. Die unverzweigte Amylose ist nicht dargestellt.
-
Charakterisiere den Bindungsmodus im Glykogen.
TippsOrientiere dich an den $CH_2-OH$-Seitenketten der Glucopyranose-Reste.
LösungDie linearen Ketten, die das Gerüst von Glykogen, aber auch von Amylopektin bilden, werden durch $\alpha-1\rightarrow 4-$glykosidische Bindungen zusammengehalten. Die beiden glykosidischen Bindungen an einem Glucose-Rest liegen sich also im Ring gegenüber, dadurch ist ein möglichst großer Abstand hergestellt. Die Kette verläuft daher linear und nicht in einem Bogen.
Die Seitenketten zweigen im rechten Winkel von dem Gerüst ab. Dies wird durch eine $\alpha-1\rightarrow 6-$-glykosidische Bindung ermöglicht. Die Seitenkette zweigt also an der $CH_2-OH-$Gruppe eines Glucoserestes ab. Diese Glucosereste haben daher glykosidische Bindungen zu drei weiteren Glucoseresten.
-
Bestimme die Abbauprodukte zu den folgenden Polysacchariden.
TippsÜberlege dir, welche Arten von Bindungen in den Polysacchariden bestehen und vergleiche dies mit den abgebildeten Disacchariden.
Ein Polysaccharid kann auch verschiedene Abbauprodukte haben.
LösungDisaccharide sind leichter zu transportieren als die großen, verzweigten Polysaccharide. Daher sind Transportformen von Kohlenhydraten oft Disaccharide. Dabei werden die Ketten vom Ende her abgebaut und in Disaccharide zerlegt. Die glykosidische Bindung zwischen den Monomeren bleibt dabei unverändert.
Cellulose besteht aus $\beta- 1 \rightarrow 4-$-verknüpften Glucose-Molekülen. Das Abbauprodukt ist dementsprechend ein Disaccharid mit der gleichen Bindung. Dies ist das mittlere der dargestellten Disaccharide, der Name ist Cellobiose.
Amylose besteht hingegen aus $\alpha-1 \rightarrow 4-$-verknüpften Glucose-Molekülen und ist unverzweigt. Daher ist das entsprechend $\alpha-1 \rightarrow 4-$-verknüpfte Disaccharid, das links dargestellt ist, das einzige Abbauprodukt. Diese Verbindung heißt Maltose.
Amylopektin und Glykogen haben zusätzlich zur $\alpha-1 \rightarrow 4-$-verknüpften Kette Seitenketten, die über $\alpha-1 \rightarrow 6-$-Bindungen mit der Kette verbunden sind. Daher gibt es ein zusätzliches Abbauprodukt, das ebenfalls eine $\alpha-1 \rightarrow 6-$-glykosidische Bindung aufweist.
-
Bestimme die Konfiguration der D-Glucopyranose.
TippsDie $\alpha$- und $\beta$-Notation bezieht sich auf die Stellung der $OH-$Gruppe am ersten Kohlenstoffatom.
$\alpha$: 1R; $\beta$: 1S
LösungDurch den Ringschluss entsteht am $C^1$-Atom ein zusätzliches chirales Zentrum. Dieses kann in R- oder in S-Konformation vorliegen, dementsprechend gibt es zwei unterschiedliche D-Glucopyranosen. Auch die daraus aufgebauten Polysaccharide zeigen unterschiedliche chemische Eigenschaften.
Liegt das erste Kohlenstoffatom in R-Konformation vor, spricht man von der $\alpha$-Form der D-Glucopyranose, liegt es in S-Konformation vor, nennt man die Verbindung $\beta$-D-Glucopyranose. Meist kürzt man die Namen aber mit $\alpha$- bzw. $\beta$-D-Glucose ab. Zwischen beiden Formen liegt ein Gleichgewicht vor, im Gleichgewicht ist die Konzentration der $\beta$-Form höher.
Aus den Regeln für die Harworth-Darstellung von Kohlenhydraten ist die Konformation des $C^1$-Atoms klar ersichtlich. Zeigt die $OH-$Gruppe nach oben, handelt es sich um die $\beta$-Form, zeigt sie nach unten, ist es die $\alpha$-Form. In der Darstellung in Sesselform entspricht die $\beta$-Form einer äquatorialen Stellung der $OH-$Gruppe und die $\alpha$-Form der axialen Stellung.
-
Erkläre den Vorteil von Glykogen als Energiespeicher im menschlichen Organismus.
TippsGibt es andere Möglichkeiten, größere Moleküle zu erhalten?
LösungIm menschlichen Organismus wird Glykogen in den Muskeln und in der Leber gelagert. Mehrere Polysaccharide sind dabei an ein Protein gebunden. Das Glykogen wird genutzt, wenn schnell viel Energie benötigt wird. Daher wird es in den Muskeln gelagert – so kann bei plötzlichen körperlichen Leistungen wie einer Flucht schnell dort Glucose freigesetzt werden, wo sie benötigt wird.
Die starke Verzweigung der Glykogen-Moleküle ist da sehr hilfreich. An jeder der Seitenketten kann gleichzeitig mit dem Abbau des Moleküls begonnen werden, so dass sehr schnell viel Glucose freigesetzt wird. So ist eine effiziente Speicherung mit schneller Verfügbarkeit der Energie verbunden. Dies ist bei Pflanzen so nicht notwendig, da diese nicht über Muskeln verfügen.

Grundbaustoffe der Nahrung – Kohlenhydrate, Eiweiße und Fette

Monosaccharide

Glucose und Fructose

Glucose – Kette oder Ring?

Monosaccharide mit 3 bis 6 C-Atomen

Monosaccharide – Nomenklatur und Stereochemie

Monosaccharide – Eigenschaften und Reaktionen

Pyranosen und Furanosen

D-Ribopyranose und D-Ribofuranose

Sesselform-Schreibweise der Pyranosen

Halbacetal- und Acetalbildung

Disaccharide

Disaccharide – Besondere Glykoside

Reduzierende und nichtreduzierende Disaccharide

Saccharose und Maltose

Polysaccharide

Polysaccharide – Cellulose, Stärke, Glykogen

Stärke und Cellulose

Nachweis von Kohlenhydraten

Moleküldarstellungen von Kohlenhydraten

Zuckerderivate
Glykoside und glykosidische Bindung

Glykolipide und Glykoproteine

Hyaluronsäure, Heparin, Chitin
9.178
sofaheld-Level
6.600
vorgefertigte
Vokabeln
7.638
Lernvideos
35.583
Übungen
32.336
Arbeitsblätter
24h
Hilfe von Lehrkräften

Inhalte für alle Fächer und Schulstufen.
Von Expert*innen erstellt und angepasst an die Lehrpläne der Bundesländer.
Testphase jederzeit online beenden
Beliebteste Themen in Chemie
- Periodensystem
- Ammoniak Verwendung
- Entropie
- Salzsäure Steckbrief
- Kupfer
- Stickstoff
- Glucose Und Fructose
- Salpetersäure
- Redoxreaktion
- Schwefelsäure
- Natronlauge
- Graphit
- Legierungen
- Dipol
- Molare Masse, Stoffmenge
- Sauerstoff
- Elektrolyse
- Bor
- Alkane
- Verbrennung Alkane
- Chlor
- Elektronegativität
- Tenside
- Toluol, Toluol Herstellung
- Wasserstoffbrückenbindung
- Fraktionierte Destillation Von Erdöl
- Carbonsäure
- Ester
- Harnstoff, Kohlensäure
- Reaktionsgleichung Aufstellen
- Redoxreaktion Übungen
- Stärke und Cellulose Chemie
- Süßwasser und Salzwasser
- Katalysator
- Ether
- Primärer Alkohol, Sekundärer Alkohol, Tertiärer Alkohol
- Van-der-Waals-Kräfte
- Oktettregel
- Kohlenstoffdioxid, Kohlenstoffmonoxid, Oxide
- Alfred Nobel
- Wassermolekül
- Ionenbindung
- Phosphor
- Saccharose Und Maltose
- Aldehyde
- Kohlenwasserstoff
- Kovalente Bindung
- Wasserhärte
- Peptidbindung
- Fermentation




 5 Minuten verstehen
5 Minuten verstehen
 5 Minuten üben
5 Minuten üben
 2 Minuten Fragen stellen
2 Minuten Fragen stellen

 Bereit für eine echte Prüfung?
Bereit für eine echte Prüfung?











